|
24 Jan |
RNA-Schalter für eine sichere Virotherapie von Krebs Allgemein, Krebs, Tumore 24. Januar 2014 Allgemein, Krebs, Tumore 24. Januar 2014
|
Krebs mit Viren zu bekämpfen – diese neue Therapieoption wird weltweit in klinischen Studien erprobt. Wissenschaftler im Deutschen Krebsforschungszentrum zeigten nun, wie sich die Sicherheit dieses Verfahrens entscheidend verbessern lässt: Ihnen gelang es erstmalig, die Vermehrung der therapeutischen Viren mit RNA-Schaltern bei Bedarf gezielt abzuschalten. Die Methode funktionierte bei Adenoviren und Masernviren, beides Kandidaten für eine Krebs-Virotherapie. RNA-Schalter könnten als zusätzlicher Sicherheitsfaktor die Virotherapie noch besser kontrollierbar machen und dadurch dem vielversprechenden Behandlungsansatz zum Durchbruch verhelfen.
In weltweit über hundert klinischen Studien untersuchen Ärzte verschiedene Viren als Waffe gegen Krebs. So prüfen Wissenschaftler im Deutschen Krebsforschungszentrum Parvoviren gegen bösartige Hirntumoren. Andernorts werden auch Adenoviren gegen Hirntumoren erprobt oder etwa Masernviren gegen Eierstockkrebs.
Bevor ein Patient mit einem therapeutischen Virus behandelt werden darf, müssen die Wissenschaftler in aufwändigen Tests minutiös darlegen, dass die Erreger beim Patienten keinerlei Krankheitssymptome hervorrufen oder gar außer Kontrolle geraten könnten. „Die Viren, die heute eingesetzt werden, haben sich als äußerst sicher herausgestellt“, sagt Privatdozent Dr. Dirk M. Nettelbeck, Virologe aus dem Deutschen Krebsforschungszentrum. „Trotzdem stellt die Sicherheit eine kontinuierliche Herausforderung dar, denn therapeutische Viren werden ständig weiterentwickelt. Oder sie müssen in höherer Dosis verabreicht werden, um Krebszellen noch effizienter abzutöten. Daher wäre es ideal, bei unerwünschten Nebenwirkungen die Viren einfach mit einem Medikament ausschalten zu können.“
Da es jedoch nur gegen wenige Viren wirksame Medikamente gibt, ist dies zum heutigen Zeitpunkt meist nicht möglich. Weltweit suchen Forscher daher nach alternativen Verfahren, um die therapeutischen Viren im Zweifelsfall unschädlich machen zu können. Dirk Nettelbecks Team setzt dabei auf bestimmte RNA-Schalter, so genannte Aptazyme. Um einen solchen Schalter zu konstruieren, fügen die Forscher synthetische DNA-Abschnitte in die Kontrollregion von Virusgenen ein, die für die Verbreitung des Erregers relevant sind. Die infizierten Zellen lesen das synthetische Konstrukt gemeinsam mit dem Gen zu einem einzigen Boten-RNA-Molekül (mRNA) ab. Der RNA-Schalter wird per Wirkstoff betätigt: Die Substanz dockt passgenau an das RNA-Molekül an und veranlasst es, sich selbst zu zerschneiden. Dadurch wird auch das Gen inaktiviert und so die Virusausbreitung gestoppt.
„Wir wollten zunächst zeigen, dass RNA-Schalter grundsätzlich geeignet sind, therapeutische Viren zu kontrollieren“, sagt Dr. Patrick Ketzer, Erstautor der Arbeit. Die DKFZ-Virologen untersuchten einen RNA-Schalter, der auf den Wirkstoff Theophyllin reagiert, an zwei verschiedenen Viren. Beide Erreger gelten als aussichtsreiche Kandidaten für die Krebstherapie, unterscheiden sich aber in ihrer Biologie: Adenoviren, deren Erbgut aus DNA besteht, und Masernviren, deren Erbinformation als RNA-Molekül gespeichert ist.
Bei den Adenoviren platzierten die Forscher den RNA-Schalter neben das Gen, das die Vermehrung des Viruserbguts in der Zelle steuert. So konnte sich die Infektion nach Zugabe des Wirkstoffs nicht mehr von Zelle zu Zelle ausbreiten. Virusinfizierte Krebszellen in der Kulturschale, etwa Melanom- oder Glioblastomzellen, produzierten nach Zugabe von Theophyllin kaum noch neue Viren, der Infektionszyklus war unterbrochen.
Bei den Masernviren schalteten die DKFZ-Virologen das Gen für das so genannte Fusionsprotein aus, das den Viren Eintritt in die Zelle verschafft. Auch in diesem Fall drosselte Theophyllin die Virusausbreitung. Damit zeigten die Forscher weltweit erstmalig, dass sich Viren mit DNA- und auch mit RNA-Erbgut durch ein Aptazym kontrollieren lassen.
„Der RNA-Schalter hat in zwei biologisch völlig verschiedenen Viren funktioniert. Deshalb gehen wir davon aus, dass dieser Ansatz sich auch zur Kontrolle anderer onkolytischer Viren eignet“, sagt Patrick Ketzer. Der Forscher denkt dabei an Erreger, die sich zwar als gute Krebs-Killer erwiesen haben, aber beim Patienten im Einzelfall Krankheitssymptome auslösen könnten. „Die Technik hat großes Potenzial, steckt aber noch in den Kinderschuhen“, sagt Dirk Nettelbeck. „Wir erwarten, dass in Kürze Aptazyme zur Verfügung stehen, die auf unterschiedliche Medikamente ansprechen und mit denen sich die Virusvermehrung vollständig unterbrechen lässt.“
Patrick Ketzer, Johanna K. Kaufmanna, Sarah Engelhardt, Sascha Bossow, Christof von Kalle, Jörg S. Hartig, Guy Ungerechts und Dirk M. Nettelbeck: Artificial riboswitches for gene expression and replication control of DNA and RNA viruses. Proceedings of the Nationals Academy of Sciences 2014, DOI: 10.1073/pnas.1318563111
Quelle: Deutsches Krebsforschungszentrum www.dkfz.de
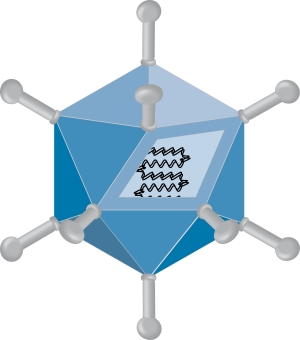
Foto-Quelle: Patrick Ketzer, DKFZ
Legende: Schematische Darstellung eines Adenovirus